2,5—二甲基—3—乙酰硫基四氢呋喃立体异构体制备及香气特征(三)
新广告法规定不得出现绝对化用词和功能性用词。我司(网站)坚决支持新广告法,积极贯彻落实新广告法要求,全力开展自纠自查,修改相关禁止词汇。
目前,公司网站整改工作正在进行中,并在此郑重声明:本网站所有页面上的绝对化用词与功能性用词在此声明前全部失效,不做理赔理由。如有不认同,请勿购买。
特此声明
9、r—2,c—5—二甲基四氢呋喃—t—3—基甲磺酸酯和r—2,t—5—二甲基四氢呋喃—t—3—基甲磺酸酯的制备
往100mL四口烧瓶内加入r—2,c—5—二甲基—t—3—羟基四氢呋喃(0.6g,5mmol)、二氯甲烷(40mL)和三乙胺(2mL,10mmol),00C下用注射器向溶液中滴加甲磺酰氯(1mL,6.5mmol),控制滴加速度,使体系温度维持在0~50C内,约30mim滴加完毕,然后室温反应12h。加入20mL水,用二氯甲烷萃取(40mLx5),合并有机相,用1mol/L的盐酸溶液(30mL)、饱和碳酸氢钠溶液(40mL)和饱和食盐水(50mL)依次洗涤,无水硫酸镁干燥。旋蒸除去二氯甲烷,将剩余物柱层析分离[硅胶柱,V(石油醚)/V(乙酸乙酯)=5:1洗脱]提纯,得到r—2,c—5—二甲基四氢呋喃—t—3—基甲磺酸酯0.91g,产率约为91%。'HNMR(CDCl3)δ1.30[6H,m,CH3(C2和C5)],1.85(1H,m,HC4),2.22(1H,ddd,J=14.1,5.1,1.5Hz,HC4),3.04(3H,s,甲磺酰基),4.10(2H,m,HC2和HC5),4.80(1H,m,HC3)。13CNMR(CDCI3)δ19.2[CH3(C5)],20.4[CH3(C2)],38.5(甲磺酰基),40.4(C4),74.3(C5),80.1(C2),85.9(C3)。HRMS(ESI):m/z[M+Na+]计算值C7H14NaO4S,217.0505;测量值:217.0505。
R—2,t—5—二甲基四氢呋喃—t—3—基甲磺酸酯通过同样的实验步骤获得,产率92%。'HNMR(CDCl3)δ1.24[3H,d,J=6.6HzCH3(C5)],1.31[3H,d,J=6.6HzCH3(C2)],1.85(1H,m,HC4),2.57(1H,m,HC4),3.04(3H,s,甲磺酰基),4.30(2H,m,HC2和HC5),4.83(1H,m,HC3)。13CNMR(CDCl3)δ18.2[CH3(C5)],21.2[CH3(C2)],38.5(甲磺酰基),39.2(C4),73.1(C5),78.5(C2),85.1(C3)。HRMS(ESI):m/z[M+Na+]计算值C7H14NaO4S,217.0505;测量值:217.0505。
10、r—2,c—5—二甲基—c—3—乙酰硫基四氢呋喃和r—2,t—5—二甲基—c—3—乙酰硫基四氢呋喃的制备
往装有温度计、磁力搅拌子的250mL三口烧瓶中加入无水碳酸钾(5.5g,0.04mol)、N,N—二甲基甲酰胺(60mL)和硫代醋酸(6mL,0.08mol),在室温下搅拌30min,用注射器向烧瓶中滴加1.9中的产物(1.9g,0.01mol)。滴加完毕后,升温至100C反应6h。冷却至室温,加入50mL乙醚,再加入50mL饱和氯化钠溶液,将混合物转移至分液漏斗中,静置分层,乙醚萃取(40mLx5),合并有机相,用50mL去离子水洗涤,无水硫酸镁千燥。旋蒸除去溶剂乙醚,将剩余粗产品柱层析提纯[硅胶柱,V(石油醚)/V(乙酸乙酯)=30:1洗脱]。得到r—2,c—5—二甲基—c—3—乙酰硫基四氢呋喃(产率82%)或r—2,t—5—二甲基—c—3—乙酰硫基四氢呋喃(产率78%左右)。r—2,c—5—二甲基—c—3—乙酰硫基四氢呋喃:'HNMR(CDCl3)δ1.21[3H,d,J=6.0HzCH3(C5)],1.28[3H,d,J=6.0HzCH3(C2)],1.51(1H,m,HC4),2.60(1H,m,HC4),2.38(3H,s,乙酰基),3.96(1H,m,HC3),4.10(2H,m,HC2和HC5)。13CNMR(CDCI3)δ17.1(CH3(C5)),21.0[CH3(C2)],30.2(乙酰基),40.4(C4),46.0(C5),73.5(C2),76.9(C3),195.3(C=O)。HRMS(ESI):m/z[M+Na+]计箅值C8H14NaO2S,197.0606;测量值:197.0606。r—2,t—5—二甲基-c-3-乙酰硫基四氢呋喃:'HNMR(CDCl3)δ1.18[3H,d,J=6.0HzCH3(C5)],1.24(3H,d,J=6.0HzCH3(C2)),2.10(2H,m,HC4),2.35(3H,s,乙酰基),3.97(1H,m,HC3),4.21(1H,m,HC5),4.35(1H,m,HC2)。13CNMR(CDCl3)δ17.1[CH3(C5)],21.6[CH3(C2)],30.7(乙酰基),41.3(C4),47.6(C5),73.2(C2),75.6(C3),195.3(C=O)。HRMS(ESI):m/z[M+Na+]计算值C8H14NaO2S,197.0606;测量值:197.0606。
二、结果与讨论
1、2,5—二甲基—3—乙酰硫基四氢呋喃立体异构体的制备及构型确认首先以丙醛和丙二酸为原料通过Knoevengael缩合得到3—戊烯酸,然后与甲基锂反应得到4—己烯—2—酮,经硼氢化钠还原后得到4—己烯—2—醇,三步反应产率分别为68%、82%和82%。三个中间体的结构均通过核磁氢谱和碳谱进行了确认,谱图数据与文献报道一致。然后在氢氧化钠的作用下环氧环开环,同时发生分子内的亲核取代反应,关环形成2,5—二甲基—3—羟基四氢呋喃,产率75%。产物的核磁氢谱和核磁碳谱中很多峰都是成对出现的,表明产物为一对立体异构体的混合物,比例大致为1:1。关环反应的机理如图3所示。由于环氧化反应为立体专一性的反应,而随后在氢氧化钠的作用下发生的环氧环开环为SN2的亲核取代,由此可以推断所得到的产物2,5—二甲基-3-羟基四氢呋喃2位甲基和3位羟基处于反式的位置,而5位的甲基相对2位的甲基则既有可能为顺式也有可能为反式的关系。因此所得的产物为4—己烯—2—醇的羟基甲磺酰化后,双键用过氧甲酸环氧化,r—2,c—5—二甲基-t-3-羟基四氢呋喃和r—2,t—5—二甲基—t—3—羟基四氢呋喃混合物。这两个立体异构体极性非常接近,无法通过柱层析分离。
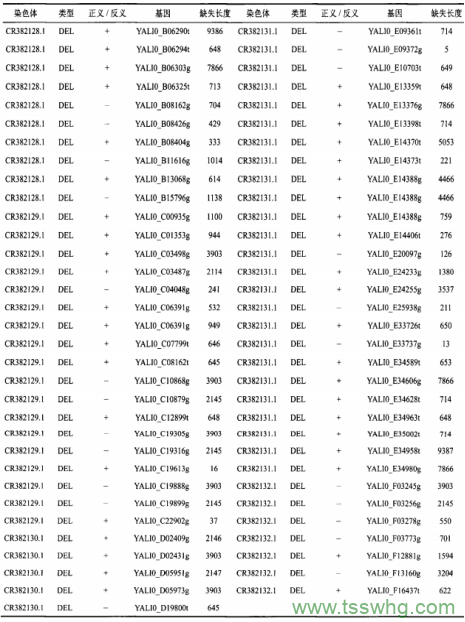
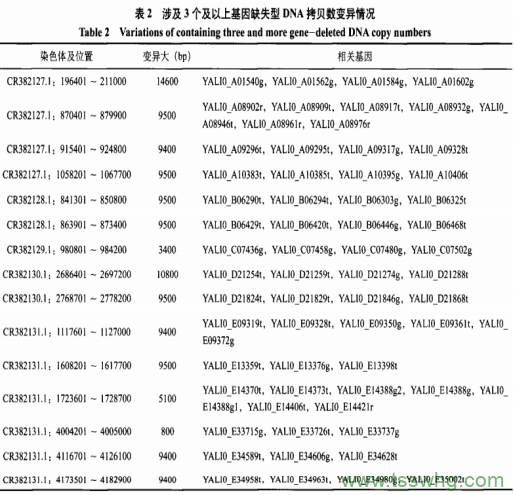
为了将r—2,c—5—二甲基—t—3—羟基四氢,呋喃和r—2,t—5—二甲基—t—3—羟基四氢呋喃两个异构体分离,本文尝试将羟基通过p—硝基苯甲酰氯转换为p—硝基苯甲酸酯,而两个异构体的p—硝基苯甲酸酯极性相差较为明显,通过柱层析分离得到r—2,c—5—二甲基四氢呋喃—t—3—基p—硝基苯甲酸酯和r—2,t—5—二甲基四氢呋喃—t—3—基p—硝基苯甲酸酯,产率分别为52%和41%。产物结构通过核磁共振谱图和高分辨质谱进行了分析,其相对立体构型通过NOE谱图得到确认。在NOE实验中,为了进行有效的判断,2号氢和5号氢的信号不能重叠。两个异构体中只有一个符合该条件,其NOE谱图如图4所示。
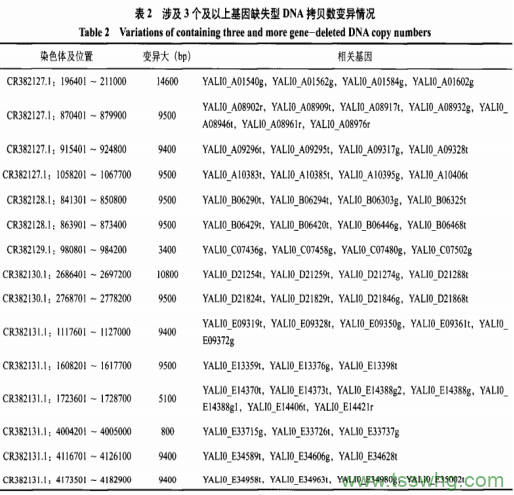
声明:本文所用图片、文字来源于《中国食品添加剂》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系。
相关链接:四氢呋喃,二氯甲烷,碳酸钾
文章版权备注
- 2023-05-01不同贮藏方式对红香酥梨采后生理及品质的影响(一)
- 2023-05-01奶味香精的制备技术与开发现状
- 2023-05-01双孢蘑菇液体菌种发酵及栽培效果浅析
- 2023-05-01菌种强化结合工艺优化提高酱香白酒基酒中四甲基吡嗪含量的研究(二)
- 2023-05-01发酵小麦胚芽产2,6-二甲氧基对苯醌菌种筛选及发酵条件优化(一)
- 2023-05-01猕猴桃中铁含量的测定与测定因素的探究
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(四)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(三)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(二)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(一)

 豫ICP备19024296号
豫ICP备19024296号 售前咨询
售前咨询